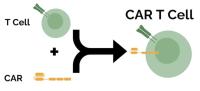
Терапия Т-клетками с химерным антигенным рецептором (CAR), несомненно, является революцией в лечении рака. Недавние успехи CAR-T-клеточной терапии в борьбе с гематологическими злокачественными новообразованиями вызвали огромный интерес к иммунотерапии. Основным направлением применения CAR-T на сегодняшний день являются лейкозы.
К лейкозам относится обширная группа заболеваний, различных по своей этиологии. При лейкозах злокачественный клон может происходить как из незрелых гемопоэтических клеток костного мозга, так и из созревающих и зрелых клеток крови.
Лейкоз выражается системной диффузной гиперплазией всего клеточного аппарата, продуцирующего лейкоциты, независимо от того, сопровождаются ли они белокровием или протекают без него. По типу течения разделяют на острые лейкозы (из незрелых клеток) и хронические (созревающие и зрелые клетки). Острые лейкозы по цитогенезу подразделяются на: лимфобластный, миелобластный, монобластный, миеломонобластный, эритромиелобластный, мегакариобластный, недифференцированный. Хронические лейкозы представлены лейкозами: миелоцитарного происхождения, лимфоцитарного происхождения и моноцитарного происхождения. Злокачественные новообразования лимфатической и кроветворной ткани в России в 2023 году составили 182,2 случая на 100 тыс. населения (~6% от всех ЗНО)
Инфраструктура для производства CAR-T клеточных индивидуальных препаратов
Что такое CAR-терапия?
Технология химерных антигенных рецепторов (CAR) вышла за пределы только Т-лимфоцитов. Учёные модифицируют и другие клетки иммунной системы, чтобы обойти ограничения классической CAR-T терапии:
- CAR-T — «золотой стандарт» для борьбы с лейкозами и лимфомами
- CAR-NK — более безопасная и доступная альтернатива на базе естественных киллеров для терапии опухолей крови и солидных форм
- CAR-M — макрофаги для «прорыва» защиты плотных солидных опухолей (рак груди, поджелудочной железы)
- CAR-Treg — регуляторные клетки для подавления иммунной агрессии при аутоиммунных болезнях и после трансплантации
Ключевое преимущество: модифицированные клетки способны размножаться и сохраняться в организме годами, обеспечивая долгосрочный противоопухолевый контроль.
Механизм действия
В основе CAR-T-терапии лежит инженерия Т-клеток, позволяющая им экспрессировать рецепторы, специально разработанные для борьбы с антигенами, связанными с раком. Например, распространенной мишенью является антиген CD19, присутствующий в В-клеточных злокачественных опухолях. Процесс включает забор Т-клеток из крови пациента с последующей их модификацией с помощью вирусных векторов (таких как лентивирус или ретровирус), которые доставляют ген CAR, создавая гибридный рецептор. Этот ген может кодировать различные домены, включая внеклеточный домен, распознающий опухолевый антиген, шарнирную область, обеспечивающую гибкость, и внутриклеточный сигнальный домен (обычно из CD3ζ и костимулирующих молекул, таких как 4-1BB или CD28) для активации Т-клеток при связывании антигена.Ключевые блоки технологической цепочки
- Молекулярно-генетический блок
- Производство CAR-клеток
- Контроль качества
- Хранение и логистика
 Клинические рекомендации и дополнительная информация
Клинические рекомендации и дополнительная информация
Дополнительные данные свидетельствуют о том, что CAR-T-терапия приносит пользу пациентам с определенными мутациями. Например, мутации в гене TP53 могут влиять на терапевтический результат. Пациенты с мутациями TP53 могут плохо реагировать на терапию из-за снижения апоптоза в раковых клетках; однако в настоящее время ведутся исследования, чтобы выяснить, можно ли разработать новые CAR-конструкции для более эффективного воздействия на эти клетки.
Кроме того, пациенты с мутациями CD19 могут представлять собой уникальную проблему. Хотя типичные CAR-T-терапии нацелены на CD19, мутации, приводящие к потере этого антигена, могут привести к побегу опухоли. Чтобы противостоять этому, в настоящее время проводятся исследования по созданию CAR-T-терапии с двойной направленностью, которая нацелена как на CD19, так и на другие специфические для В-клеток антигены, такие как CD20 или CD22.
CAR-T-терапия символизирует смену парадигмы в онкологии, особенно для тех, кто борется с трудноизлечимыми раковыми заболеваниями. Благодаря тщательному изучению генов-мишеней и мутаций, эта область готова к значительным достижениям, способствующим персонализированному лечению рака. По мере развития технологий и углубления нашего понимания CAR-T-терапия может распространиться не только на гематологические злокачественные опухоли, но и на солидные опухоли, давая надежду более широкому кругу пациентов. Продолжающиеся исследования и клинические испытания, несомненно, позволят определить ее роль и раскрыть весь ее потенциал в лечении рака.