Мероприятия
Новая эра Т-клеточной терапии при меланоме.
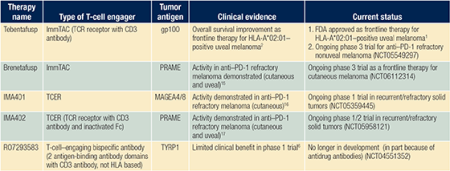
Терапия ингибиторами иммунных контрольных точек значительно улучшила результаты лечения пациентов с метастатической меланомой. Однако у части пациентов с меланомой кожи не наблюдается реакции на стандартные ингибиторы контрольных точек. Кроме того, пациенты с редкими подтипами меланомы, такими как увеальная меланома, с меньшей вероятностью получат пользу от лечения. Терапия, направленная на активацию Т-клеток, — это новый класс иммунотерапии рака, который расширяет возможности противоопухолевого иммунитета. Tebentafusp, мобилизующий иммунитет моноклональный TCR против рака (ImmTAC), нацеленный на gp100, показал общее улучшение выживаемости при увеальной меланоме и в настоящее время является одобренной FDA передовой терапией. Агенты, воздействующие на Т-клетки, нацеленные на другие опухолевые антигены (PRAME, MAGEA4), в настоящее время исследуются в ходе клинических испытаний, и разрабатываются совершенно новые платформы, воздействующие на Т-клетки.
В широком смысле активаторы Т-клеток представляют собой молекулы, у которых есть один домен, связывающийся с мишенью, связанной с раком, и другой домен, связывающийся с Т-клеткой. Домен, связывающийся с Т-клеткой, обычно представляет собой моноклональное антитело анти CD3. Для связывания с опухолью в первых одобренных активаторах Т-клеток использовались фрагменты антител против антигенов клеточной поверхности. При гематологических злокачественных новообразованиях этот подход доказал свою эффективность, получив одобрение FDA для Т-клеточных активаторов, нацеленных на CD19, CD20, BCMA и GPRC5D. В солидных опухолях тарлатамаб (нацеленный на DLL3) был недавно одобрен для лечения мелкоклеточного рака легкого, и есть несколько примеров Т-клеточных активаторов на основе антител, находящихся в стадии разработки при раке предстательной железы (NCT06691984). Однако для многих солидных опухолей идентификация антигенов-мишеней с опухолевой специфичностью остается сложной задачей, и Т-клеточные активаторы на основе антител нацелены на методы лечения, вовлекающие клетки, которые могут быть ограничены чрезмерной токсичностью или недостаточной эффективностью.
В качестве альтернативы подходам, основанным на использовании антител, TCR нацелены на пептиды — главные комплексы гистосовместимости (ГКГС/HLA), которые экспрессируются на поверхности опухолевых клеток. Пептиды включают фрагменты внутриклеточных белков, что существенно расширяет спектр антигенов, на которые можно воздействовать. Кроме того, взаимодействие между TCR и пептидами — ГКГС является высокоспецифичным, что позволяет точно воздействовать на опухолевые клетки, ограничивая при этом токсическое воздействие на нецелевые клетки. Tebentafusp - это первый в своем классе ImmTAC, который сочетает растворимый TCR, нацеленный на gp100, с фрагментом антитела CD3. Доклинические исследования показали, что Tebentafusp может поражать клетки меланомы, содержащие всего 10 молекул пептида gp100-MHC на клетку. Основным ограничением терапии на основе TCR является требование соответствия конкретному подтипу HLA пациента — в данном случае HLA-A * 02:01.
Ref:
- 1. U.S. Food and Drug Administration. FDA approves tebentafusp-tebn for unresectable or metastatic uveal melanoma. Fda.gov. January 25, 2022. Updated January 26, 2022. Accessed July 3, 2025. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-tebentafusp-tebn-unresectable-or-metastatic-uveal-melanoma.
- Hassel JC, Piperno-Neumann S, Rutkowski P, et al. Three-year overall survival with tebentafusp in metastatic uveal melanoma. N Engl J Med. 2023;389(24):2256-2266.
- Goebeler M-E, Stuhler G, Bargou R. Bispecific and multispecific antibodies in oncology: opportunities and challenges. Nat Rev Clin Oncol. 2024;21(7):539-560.
- 4. U.S. Food and Drug Administration. FDA grants accelerated approval to tarlatamab-dlle for extensive stage small cell lung cancer. Fda.gov. May 16, 2024. Accessed July 3, 2025. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-tarlatamab-dlle-extensive-stage-small-cell-lung-cancer.
- Kebenko M, Goebeler ME, Wolf M, et al. A multicenter phase 1 study of solitomab (MT110, AMG 110), a bispecific EpCAM/CD3 T-cell engager (BiTE®) antibody construct, in patients with refractory solid tumors. OncoImmunology. 2018;7(8):e1450710.
- Spreafico A, Couselo EM, Irmisch A, et al. Phase 1, first-in-human study of TYRP1-TCB (RO7293583), a novel TYRP1-targeting CD3 T-cell engager, in metastatic melanoma: active drug monitoring to assess the impact of immune response on drug exposure. Front Oncol. 2024;14:1346502.
- Liddy N, Bossi G, Adams KJ, et al. Monoclonal TCR-redirected tumor cell killing. Nat Med. 2012;18(6):980-987.